 欢迎来到北京博奥森生物技术有限公司网站!
欢迎来到北京博奥森生物技术有限公司网站! 欢迎来到北京博奥森生物技术有限公司网站!
欢迎来到北京博奥森生物技术有限公司网站!
减一对照
在多色流式实验中,荧光溢漏是导致通道信号难区分、设门不准确的核心原因。随着检测指标增多,荧光素光谱重叠的概率增加,单一荧光的溢漏会被多色叠加放大,整体荧光溢漏情况持续变化——这种情况下,未染色的空白对照(未涉及荧光溢漏干扰)或全通道同型对照(无法覆盖多色交叉溢漏)均无法模拟全染背景,尤其对分群不明显、低表达量指标(需从大量阴性群体中识别阳性信号),必须依赖减一对照(FMO对照,Fluorescence Minus One)排除干扰。减一对照,又称荧光扣除对照或圈门对照,是多色流式分析中针对特定通道的阴性对照。其操作逻辑为:对目标通道不进行荧光染色,其余所有检测通道均按目标样本的染色方案完整染色,以此模拟“全染背景下,仅目标通道无特异性信号"的场景。
该对照主要应用于:研究不同细胞亚群的表型分子(如免疫细胞表面标志物)、细胞因子等指标的检测,尤其适用于多色(≥3色)实验或低表达指标分析。
减一对照的核心作用
1.排除全染背景干扰:通过“缺失一个通道荧光",直观区分“目标通道的特异性信号"与“其他通道溢漏至该通道的非特异性信号";
2.评估荧光溢漏程度:量化其他荧光染料向目标通道的溢漏比例,为补偿调节和设门提供精准依据;
3.确保设门准确性:在低表达、分群模糊的场景中,明确阴性群体的信号边界,避免因溢漏信号误将阴性细胞判定为阳性。
减一对照注意事项
死细胞对照
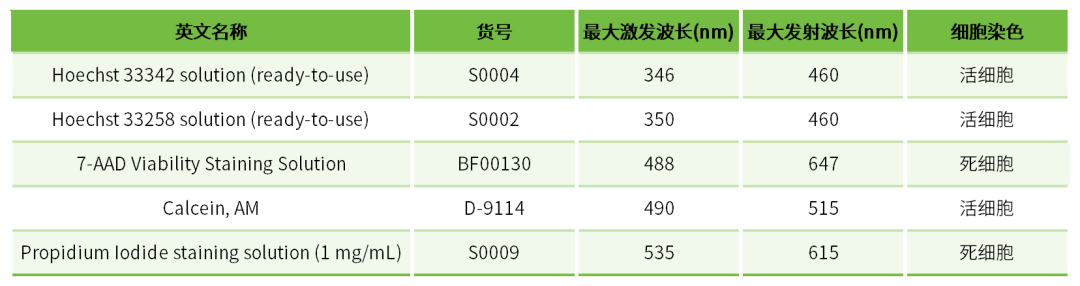
样本中死细胞的存在会极大地影响染色效果,因为死细胞具有更大的自发荧光,而且会增加非特异性的抗体结合,导致假阳性并增加背景信号,降低阳性信号的动态范围,这可能会使弱阳性样本和稀有细胞群体的鉴定变得困难。还可能会释放DNA,DNA非常黏稠,会导致细胞成团,容易堵塞管路。此外,死细胞无法刺激表达活化功能相关的标志物,从而导致一些比真实阳性率低的假阴性结果产生。使用基于FSC和SSC的门可以帮助清除部分碎片和死细胞,但无法全部移除,因此需要借助灵敏且特异性的染料对细胞进行活性分析。其原理是利用细胞死亡后的通透性改变来做特异性荧光标记,常见染料包括DNA染料类,分为两种,一种是膜不透过性染料(如PI、7-AAD),仅标记死细胞;另一类是膜透过性染料(如 Hoechst 33342),可标记活细胞核,常用于活细胞示踪或与 PI 联合使用进行死活双染。而荧光标记的Annexin V检测凋亡细胞,可结合外翻的磷脂酰丝氨酸。此外,还可以通过对细胞大小变化及理化性质的测定进行细胞活性检测。
其它实验对照
其它实验对照,用于比较特定实验条件下样本之间的差别,主要分为以下几个类别:
1.阴性对照能够提供所有待测标志物的表达背景,用于比较细胞经过化学或生物学处理后的蛋白表达差异,例如细胞内染色实验涉及固定和破膜,这些步骤会影响抗原检测、自发荧光、荧光染料亮度和细胞形态。
2.阳性对照用于证实抗体在相关细胞中的阳性染色,以表明抗体在实验中起作用。
3.纵向对照/参考对照是长期研究的质量控制,可以确保实验过程中的染色一致性。